дозировка и применениеКлинические исследования
клинические исследования coronaКлиническое исследование III фаза
Клиническое исследование III фаза
CORONA
Многоцентровое двойное слепое плацебо-контролируемое с адаптивным дизайном рандомизирован-ное клиническое исследование, фаза III
Цель:
изучить показатели эффективности и безопасности препарата левилимаб у субъектов с тяжелым течением COVID-19.
Критерии включения:
лица 18 лет и старше, госпитализированные с тяжелой формой новой коронавирусной инфекции (COVID-19), получающие стандартную терапию.
Включенные пациенты:
- средний возраст 58 лет;
- с избыточной массой тела (ИМТ = 29,5);
- с длительной лихорадкой ≈ 10 сут.;
- продолжительность пневмонии ≈ 5 сут.;
- госпитализированные и получающие оксигенотерапию в течение ≈ 4 сут.
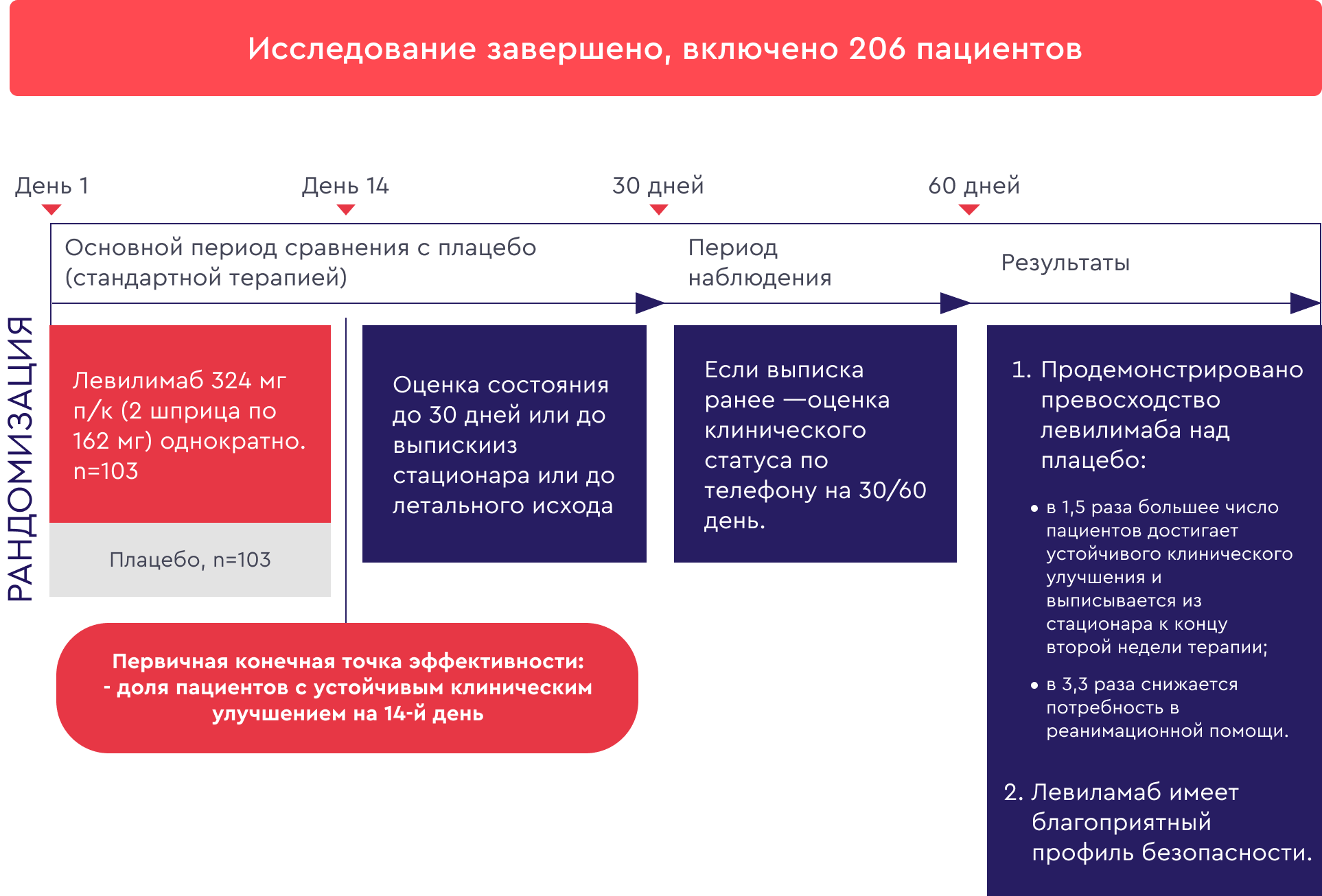
При отсутствии эффекта назначается «терапия спасения»:
Открытое введение левилимаба 324 мг подкожно при клиническом ухудшении или отсутствии улучшения в течении COVID-19 после введения исследуемого препарата.
Клиническая эффективность
Доля пациентов с устойчивым клиническим улучшением, %
На 14-й день после однократного введения левилимаба в 1,5 раза больше пациентов достигло устойчивого клинического улучшения по сравнению с группой плацебо.
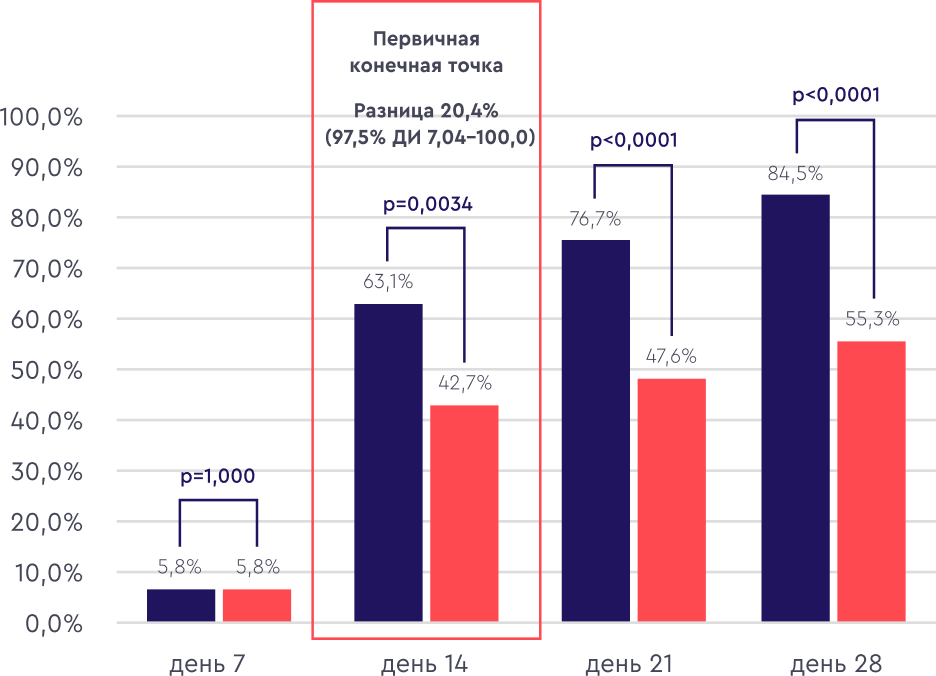
левилимаб (n=103)плацебо (n=103)
Доля выписанных пациентов, %
После однократного введения левилимаба начиная с 13-го дня большее количество пациентов было выписано из стационара по сравнению с группой плацебо.
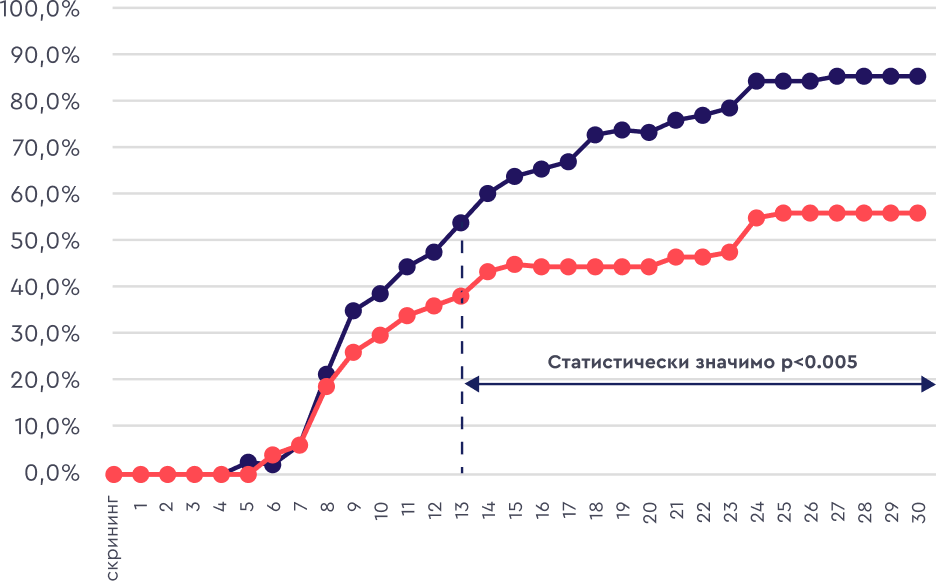
левилимаб (n=103)плацебо (n=103)
После однократного введения левилимаба в 3,3 раза реже требовался перевод в отделение реанимации по сравнению с группой плацебо (2,9 vs 9,7%, р = 0.04).
При исходном введении левилимаба в 3 раза реже была необходимость его дополнительного введения в качестве «терапии спасения», чем в группе плацебо (12,6 vs 40,8%, р < 0.0001).
Основные результаты
Заключение по
эффективности
эффективности
- Исследование подтвердило превосходство левилимаба по сравнению с плацебо в отношении достижения устойчивого клинического улучшения.
- Однократное введение левилимаба пациентам с тяжелой формой COVID-19в 1,5 раза увеличивает частоту достижения устойчивого клинического улучшения и выписки из стационара, а также в 3,3 раза снижает частоту перевода пациентов в ОРИТ.
Заключение по
безопасности
безопасности
- Левилимаб в дозе 324 мг однократно и двукратно имеет благоприятный профиль безопасности, соответствующий известным данным о группе ингибиторов рецепторов интерлейкина-6 (ИЛ-6).
- Повышения частоты значимых бактериальных инфекций не наблюдалось.
- Наиболее частые нежелательные реакции: повышение АСТ/АЛТ, повышение АД, нейтропения —наблюдались преимущественно легкой и умеренной степени (1–2 ст.).
Ингибирование сигнального пути ИЛ-6 с помощью левилимаба является эффективным методом лечения у пациентов с новой коронавирусной инфекцией.
Источники
- ИМП препарата ИЛСИРА® Data on file. Отчет о КИ BCD-089-1.
- Адаптировано: Jamilloux Y. et al. Autoimmuniti Reviews. Available online 4 May 2020, 102567. https://doi.org/10.1016/j.autrev.2020.102567.
- JAMA. 2020;323(15):1499-1500. doi:10.1001/jama.2020.3633
- Согласно Временным методическим рекомендациям МЗ РФ. «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID–19)».
- Lomakin, N.V., Bakirov, B.A., Protsenko, D.N. et al. The efficacy and safety of levilimab in severely ill COVID-19 patients not requiring mechanical ventilation: results of a multicenter randomized double-blind placebo-controlled phase III CORONA clinical study. Inflamm. Res. (2021). https://doi.org/10.1007/s00011-021-01507-5